【共通テスト対策】酸化数の求め方|文系のための高校化学基礎
酸化還元の単元がよくわからない…
テスト対策・共通テスト対策をしたいけど何からすればよいのか…
このような方にまず会得してもらいたいのが
「酸化数」の求め方。
酸化数は簡単なルールと解法の手順を身に付けることで、
簡単に求められるようになります。
さらに、酸化数が求められるようになると、
それに連動して酸化還元の様々な問題が解けるようになるので、
習得のコスパ◎です!
酸化数って何?
酸化数って何に使う?
酸化数を求めるためのルールは?
実際に酸化数を算出する
この記事では「酸化数の計算方法」を、
化学が苦手な文系の高校生にもわかりやすく解説をします。
化学基礎の定期テスト・共通テストの突破を目指して、
この記事で酸化数を完ぺきにしましょう!
酸化数って何?(詳しく説明|初見はスルーOK!)

酸化数が何なのか気になる人はここから読んでください。
とりあえず最短で化学基礎をおさえたい方は、次の見出しからでOKです!
酸化数とは、
その原子が電子をどれだけ失った(または受け取った)かを表す数
です。
その原子が電子を1つ失うと酸化数は1増えて、
電子を一つ受け取ると酸化数は1減ります。
ところで、酸化還元と電子の関係は覚えていますか?
電子を失うとその原子は酸化、電子を受け取ると還元される。
これが酸化還元と電子の関係です!
「酸化数の定義」と「酸化還元と電子の関係」を組み合わせると…
酸化数が増えるとその原子は酸化、酸化数が減るとその原子は還元される。
という関係を導くことができます。
酸化数って何に使う?(初見はここから!)

これから酸化数の計算方法を学習する前に、
まずは酸化数について学ぶメリットを見ておきましょう。
酸化数の役割は、
反応の前後でその物質が酸化・還元されたかを判定することです。
反応の前後で酸化数が増えていたら、その物質は酸化されている。
このように、酸化還元のチェッカーとして酸化数を使います。
例)
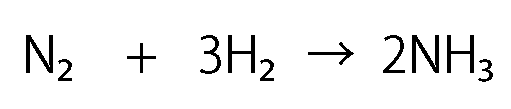
この反応について、酸化数を計算してみると…
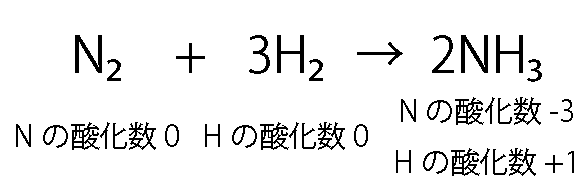
よって
よって
このように、酸化数はその物質が酸化・還元されたかをチェックするために使います。
酸化数の実践的な使用方法はまた別の記事で詳しく説明します。
この記事ではまずは土台として、酸化数の計算方法について学習しましょう。
酸化数の計算のために覚えるルール

■ 酸化数の計算の前提
酸化数は単体・化合物の各元素について数値です。
NH₃ について考える場合は、
NH₃ のN の酸化数は○○で、Hの酸化数は○○だ!
のように一つ一つの元素について数値を求めます。
この「一つ一つの元素について」というところを頭に入れて先に進んでください!
ではここから「酸化数を計算するためのルール」を解説します。
まずは単体・化合物・イオンの全体の酸化数について説明します。
これはおそらく感覚とも一致するはずです。
気楽に3つ覚えましょう!
■ ルール① 単体の酸化数は0
- H₂ → (Hの酸化数)=0
- O₂ →( Oの酸化数)=0
■ ルール② 化合物全体の酸化数の和は0
H₂O → (Hの酸化数)×2+(Oの酸化数)=0
NH₃→(Nの酸化数)+(Hの酸化数)×3=0
H₂O はHが2粒でOが1粒、というように考えてください!
■ ルール③ イオンの酸化数は「電荷と一致」
例:
- SO₄²⁻ → (Sの酸化数)+(Oの酸化数)×4=ー2
- NH₄⁺ → (Nの酸化数)+(Hの酸化数)×4=+1
ルール①~③について、あえて雑な説明をすると…
ひとつのかたまり(単体・化合物・イオン)について、
各元素の酸化数の和=かたまりの右上に書いてある数
と思ってくれればOKです!
MnO₄⁻ であれば (Mnの酸化数)+(Oの酸化数)×4=ー1
このように考えます!
ここまでは分かるけど、でもこれじゃあ各元素の酸化数が分からない…
そのために、ここから先は元素ごとのルールを覚えます!
これらは一つ一つ暗記しましょう!
■ ルール④ 化合物中のH(水素)は原則+1
化合物中のH(水素)の酸化数は原則+1です。
例:
- H₂O → (水素の酸化数)=+1
- HCl →(水素の酸化数)=+1
例外:
- NaH → (水素の酸化数)=-1
- CaH₂→ (水素の酸化数)=-1
金属と結合する場合は、水素の酸化数はー1です。
このような例外も覚えておきましょう。
■ ルール⑤ 化合物中のO(酸素)は原則ー2
化合物中のO(酸素)の酸化数は原則-2です。
例:
- H₂O → (Oの酸化数)=-2
- CO₂ → (Oの酸化数)=-2
例外:
- H₂O₂ → (Oの酸化数)=-1
- BaO₂ → (Oの酸化数)=-1
O₂²⁻(過酸化物イオン)を含む場合は −1 です。
特に過酸化水素(H₂O₂ )は定期テストでも頻出なので覚えておきましょう。
■ ルール⑥ 電離したときの価数=酸化数
H, O 以外にも覚える覚えるべき元素が多く存在するのですが、
これらは、「電離したときの価数=酸化数」と覚えればOKです!
アルカリ金属元素
化合物中のLi, Na, K などは、
共通テスト範囲では化合物中で必ず +1です!
ハロゲン元素
化合物中のF, Cl, Br, I は
基本的に ー1です!
(※酸素と結合する場合などの例外は発展内容)
酸・塩基
- HNO₃ → H⁺ + NO₃⁻
(Hの酸化数)=+1、(NO₃ 全体の酸化数)=ー1
- Al₂(SO₄)₃ → 2Al ³⁺+ 3SO₄²⁻
(Alの酸化数)=+3、(SO₄²⁻ 全体の酸化数)=ー2
問題のレベルが上がってくると硫酸イオン(SO₄²⁻)などの酸化数も問われるので、
そのようなときはこのように電離の式を思い出しましょう!
以上が酸化数の計算のために覚えるべきルールです!
周期表や酸・塩基の単元がバッチリな方にとってはかなり覚えやすいルールではないでしょうか。
化学基礎は前後の単元が今の単元に干渉してくる科目です。
そのため、今習っている単元以外(特にこれより前の単元)に穴があると、
どうしても高得点の確保は難しくなります…
周期表や酸・塩基があいまいな方は、
一度それらを復習して、再度ここに戻ってくることをおすすめします!
ここから先は、今覚えたルールを使って、
実際に各元素の酸化数を計算してみましょう!
分子・多原子イオン中の原子の酸化数の求め方

実際の試験では、ルール④~⑥で登場した元素以外について、
その酸化数を問われることが多いです。
それらの元素については、
個別に数値を暗記するのではなく、今から紹介する計算で酸化数を求めます!
- 問われている元素の酸化数を x と置く
- 酸化数が分かるものを埋める
(H・O・アルカリ金属など) - 全体の和=0(または電荷)で式を立てる
- 方程式を解く
この手順を用いてNH₃, NO₃⁻ 中の窒素原子の酸化数を求めてみましょう。
NH₃のNの酸化数を求める
- 問われている元素の酸化数を x と置く
- 酸化数が分かるものを埋める
(H・O・アルカリ金属など) - 全体の和=0(または電荷)で式を立てる
- 方程式を解く
この手順に従って実際に求めます。
問われている元素をxと置く・分かるものを埋める
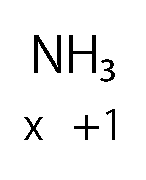
手順1と2は分離するとかえってややこしいので、まとめてしまいます。
今回はN について問われているので、Nの真下にxを書きます。
Hの酸化数は原則+1なので、Hの真下に+1を書きます。
このように、
かたまり(単体・化合物・イオン)の各元素の真下にxや数値を書きこみましょう!
全体の和=0(または電荷)で式を立てる
(NH₃全体の酸化数)=0
ここから方程式が立てられます。
方程式を解く
この方程式を解くと
よって、NH₃中のNの酸化数は-3です。
NO₃⁻ のNの酸化数の求め方
- 問われている元素の酸化数を x と置く
- 酸化数が分かるものを埋める
(H・O・アルカリ金属など) - 全体の和=0(または電荷)で式を立てる
- 方程式を解く
この手順に従って実際に求めます。
問われている元素をxと置く・分かるものを埋める
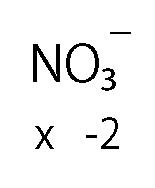
問われているNの酸化数をxとおきます。
酸素の酸化数は原則ー2なので、それを用いましょう。
全体の和=0(または電荷)で式を立てる
(NO₃⁻の酸化数の和)=-1なので
ここから方程式が立てられます。
方程式を解く
この方程式を解くと
よって、NO₃⁻中のNの酸化数は+5です。
まとめ
酸化数の計算方法はうまくつかめましたか?
まずは計算のためのルールをしっかりと覚える!
ルールを覚えたら、今度は数値を書き込んで方程式を立てて計算。
化学の試験は時間との勝負です。
酸化数の計算はスムーズに解けるまで繰り返し演習をしましょう!
酸化数の計算は、繰り返し練習してスムーズにこなせるようにしましょう。
実際に自分の手を動かして、例題や学校ワークの問題をよく練習してください!
次に読むべき記事
酸化数が理解できたら、次にやるべきことは1つです。
酸化還元反応の見抜き方です。
「この反応は酸化還元反応である。〇か×か」
酸化数を実際に活用する単元へと進みましょう!
酸化数の特定のためには、
周期表や酸・塩基の知識がかなり重要でしたね。
化学基礎は前後の単元が今の単元に干渉してくる科目です。
そのため、今習っている単元以外(特にこれより前の単元)に穴があると、
どうしても高得点の確保は難しくなります…
周期表や酸・塩基があいまいな方は、
一度それらを復習して、再度ここに戻ってくることをおすすめします!

